Основная цель эндодонтического лечения заключается в очистке и дезинфекции всей длины корневого канала. Неправильная очистка канала, главным образом в апикальной трети, может стать причиной серьезных ошибок. В клинических случаях с патологическим смещением апикального отверстия III типа, как правило, не удается добиться качественной очистки и дезинфекции с применением стандартных методов пломбирования. Поэтому вышеуказанные этапы должны быть выполнены с применением апикальной микрохирургии для удаления необработанных областей и ретроградной герметизации.
The main purpose of endodontic treatment is to clean and disinfect the entire length of the root canal. Improper cleaning of the channel, mainly in the apical third, can cause serious errors. In
cases with abnormal clinical apical foramen III displacement type is generally not possible to achieve high-quality disinfection and purification using standard filling techniques. Therefore, the above steps should be performed using microsurgery apical to remove rough areas and retrograde sealing.
Эндодонтия – специальность, которая занимается профилактикой и лечением патологий пульпы верхушечного периодонтита. Основная цель эндодонтического лечения заключается в очистке и дезинфекции всей длины корневого канала до достижения уровня здоровых тканей [10]. Благодаря тщательной и кропотливой обработке такая цель достижима и процент успешного лечения может превышать 94% [6, 7].
Залог успеха эндодонтического лечения – механическая обработка, осуществляемая эндодонтическими инструментами и химическими ирригационными растворами.
После очистки и формования эндодонтический пломбировочный материал должен трехмерно заполнить пространство каналов, предотвращая повторное апикальное инфицирование и сохраняя асептические условия, достигнутые на предыдущих этапах лечения. Механическое препарирование системы корневых каналов имеет первостепенное значение в процессе эндодонтических дезинфекций [1]. Оно отвечает за физическое удаление инфицированного дентина и содержащихся в дентинных каналах бактерий, а кроме того, увеличивает диаметр магистральных каналов, обеспечивающих поступление большего объема оросительных растворов в апикальную треть [9, 10], и создает благоприятную коническую форму для пломбирования каналов. Таким образом, от этого этапа во многом зависит качество дезинфекции.
Процедурные ошибки во время механической фазы препарирования могут сделать невозможным достижение необходимого уровня дезинфекции. W. Yousuf с соавт. в 2015 г. провели цифровое рентгенографическое исследование 1748 зубов во время эндодонтического лечения и обнаружили процедурные ошибки в 32,8% случаев (574 зубов). Одна из наиболее распространенных – смещение апикального отверстия, особенно в искривленных каналах [2–4]. Согласно глоссарию эндодонтических терминов Американской ассоциации эндодонтистов смещение каналов определяется как удаление стенки по внешней кривизне апикального канала в связи с тенденцией файлов восстанавливать первоначальную линейную форму во время препарирования, что может привести к образованию уступа или возможной перфорации.
Непреднамеренное использование жестких стальных эндодонтических файлов, особенно большого диаметра, без учета анатомии канала увеличивает риск транспозиции апикального отверстия.
Неправильная очистка канала, главным образом в апикальной трети, может стать причиной ошибки [8, 11]. Смещение апикального отверстия не только ухудшает дезинфекцию системы каналов и затрудняет доступ к естественной топографии канала, но и вызывает раздражение тканей из-за выдавливания в периодонт растворов, содержащих бактерии, и остатков продуктов их распада. Также затруднена корректная припасовка апикального гуттаперчевого стержня, что впоследствии отрицательно повлияет на апикальную герметизацию и инфекционный контроль [12]. В результате может резко ухудшиться клинический прогноз лечения.
Согласно A.H. Gluskin с соавт. смещение апикального отверстия можно разделить на три типа [5]:
I – незначительное смещение естественного физиологического положения отверстия.
II – умеренное смещение естественного физиологического положения отверстия, в результате чего происходит значительное ятрогенное смещение по внешней кривизне корня и образуется достаточно большое сообщение с периапикальным пространством.
III – грубое разрушение естественной физиологической позиции апикального отверстия канала, приводящее к значительной ятрогенной патологии. Благоприятный успех лечения в этих случаях достигается с помощью комбинированных клинических методов.
Каналы с патологий смещения I типа, как правило, могут быть очищены и заполнены обычным способом.
При патологии II типа необходимо создание апикального барьера с размещением апикальный пробки из МТА для контроля кровотечения или экссудации и создания своего рода щита, способного предотвратить выталкивание эндодонтического пломбировочного материала в периодонт. После этого выполняют эндодонтическое пломбирование по выбранной методике.
В клинических случаях с патологическим смещением апикального отверстия III типа обычно не удается добиться качественной очистки и дезинфекции стандартными методами пломбирования. Поэтому вышеуказанные этапы должны быть выполнены с применением апикальной микрохирургии для удаления необработанных областей и ретроградной герметизации.
Клинический случай
Пациентка, 55 лет, обратилась в стоматологическое отделение с жалобами на постоянную боль, обостряющуюся во время жевания и пальпации в апикальной области зубов 11 и 13, которые в последние 3 мес были подвергнуты эндодонтическому лечению. Кровяное давление пациентки – 128 х 78 мм рт. ст., частота сердечных сокращений – 82 уд/мин, насыщение кислородом – 98%, температура тела – 38,5 °С.
Женщина сообщила, что не чувствовала боли перед началом первичного эндодонтического вмешательства, и это было указано в плане реабилитационного лечения. На 3-й день после первой сессии эндодонтического лечения, когда одновременно были обработаны зубы 11 и 13, боль начала усиливаться. На 4-й день для контроля боли пациентке назначили внутривенное введение анальгина и кетопрофена.Параллельно с систематическим лечением провели окклюзионную корректировку. Через 2 дня боль возобновилась, и пациентка вынужден была обратиться к другому стоматологу, который назначил введение анальгина натрия по 500 мг/мл каждые 4 ч и нимесулида 100 мг каждые 12 ч перорально в течение 7 дней. Боль уменьшилась, но не прекратилась. Через 2 дня после окончания применения системных препаратов женщина снова ее почувствовала. Она обратилась к третьему специалисту, который инициировал повторное эндодонтическое вмешательство на зубах 11 и 13. Тем не менее после терапии боль не исчезла. Через 4 дня у пациентки появилось лихорадочное состояние с повышением температуры. Установлено, что ни в одном из случаев эндодонтического лечения не было создано необходимых условий для герметизации.
Клиническое обследование выявило неадекватную конфигурацию эндодонтического доступа в зубах 11 и 13 и недостаточную химико-механическую обработку системы корневого канала (рис. 1, 2).
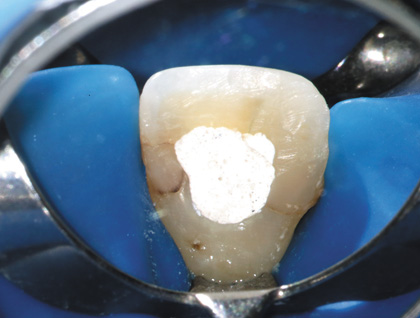
Рис. 1 Зуб 11: начальная клиническая ситуация
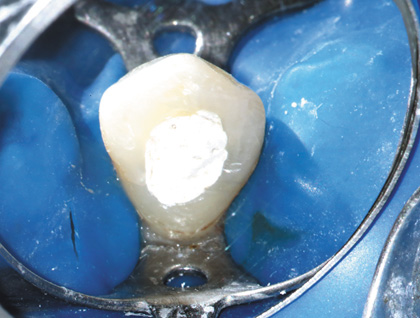
Рис. 2 Зуб 13: начальная клиническая ситуация
Эндодонтическое перелечивание началось с установления ретроградной патологии с апикальным смещением III типа. На зубе 12 была полная металлическая коронка, внутри – корневой штифт. Эндодонтическое лечение выполнено плохо (рис. 3). На томографии определили транспозицию отверстия на зубах 11 и 13 (рис. 4, 5). Из-за сложности апикального смещения на данных зубах рекомендовано повторное эндодонтическое лечение с применением микрохирургических методов. Необходимо было и лечение зуба 12 с очисткой, формированием системы каналов и их дезинфекцией с последующим пломбированием. Но так как на этом зубе была установлена хорошо адаптированная коронка, а на соседних зубах запланирована микрохирургическая операция, принято решение об эндодонтическом ретроградном лечении зуба 12.
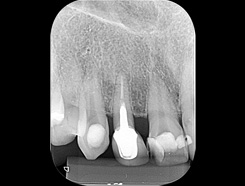
Рис. 3 Первичная рентгенограмма
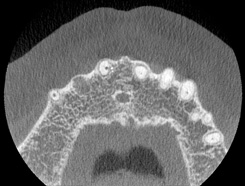
Рис. 4 Томографическое изображение, демонстрирующее смещение апикального отверстия зуба 11
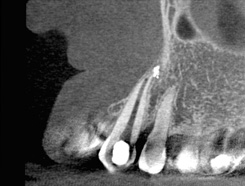
Рис. 5 Томографическое изображение, демонстрирующее смещение апикального отверстия зуба 13
Начато повторное эндодонтическое лечение зуба 11, затем зуба 13. Каналы препарировали вращающимися файлами Reciproc 50 (VDW, Мюнхен, Германия) и орошали 2,5%-ным раствором гипохлорита натрия
и 17%-ным раствором ЭДТА с использованием дополнительной активации ультразвуковыми инструментами. С помощью операционного микроскопа и периапикального рентгеновского исследования определили апикальное смещение зуба 11, однако не удалось установить оригинальную траекторию просвета апикальной части каналов (рис. 6, 7). То же самое наблюдали в зубе 13. В связи с большими изменениями толщины стенок каналов после смещения отверстия не удалось выполнить правильную припасовку гуттаперчевого конуса. Поэтому было решено создать апикальную пробку 4 мм с помощью MTA-HP (Angelus, Лондрина, Бразилия, рис. 8).
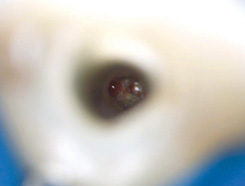
Рис. 6 Клиническое изображение через микроскоп, демонстрирующее оригинальную траекторию каналов и апикальную патологию в зубе 11
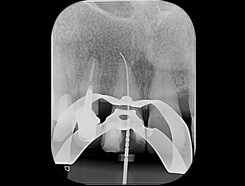
Рис. 7 Рентгенологическое изображение эндодонтического файла, расположенного в области апикальной патологии
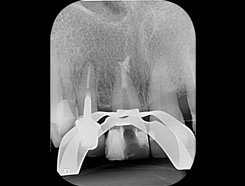
Рис. 8 Апикальная пробка из MTI-HP (Angelus, Лондрина, Бразилия)
Остальную часть каналов заполнили термопластифицированной гуттаперчей с силером Fillapex MTA – эндодотническим пломбировочным материалом, содержащим частицы МТА.
После этого пациентке проведена апикальная микрохирургическая операция: соответствующая апикальная область удалена пьезоэлектрическим ультразвуком и наконечником W1-CVDentus. На зубе 12 выполнена апикоэктомия теми же инструментами, канал ретроградно подготовлен, высушен хирургическим наконечником для отсасывания Endo Tips 0.014″ (Angelus, Лондрина, Бразилия) и ретроградно запломбирован с помощью MTA-HP (Angelus, Лондрина, Бразилия, рис. 9–11).
MTA-HP – материал выбора для герметизации ретроградным пломбированием и заполнения апикальной трети канала при резекции корня. Он обладает превосходными характеристиками краевой адаптации. Биосовместимость, уплотнительная способность во влажной среде, индуцирование формирования твердых тканей делают его наиболее подходящим в подобных клинических ситуациях. MTA состоит из порошка и жидкости. Сохранив все преимущества традиционного MTA, он стал проще в клиническом применении благодаря изменению размера частиц порошка и добавлению пластификатора к жидкости.
Через 5 мес после микрохирургического вмешательства рентгенологически установлено быстрое восстановление и заживление в переапикальных тканях зубов 11, 12 и 13 (рис. 12). Пациентка не имела каких-либо жалоб на боль и была удовлетворена лечением.
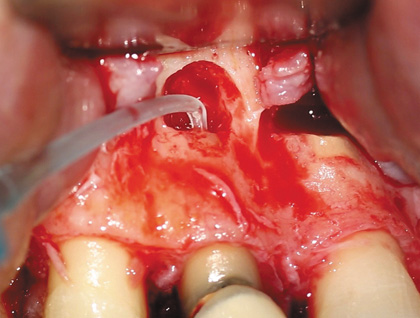
Рис. 9 Высушивание канала зуба 12 хирургическим наконечником
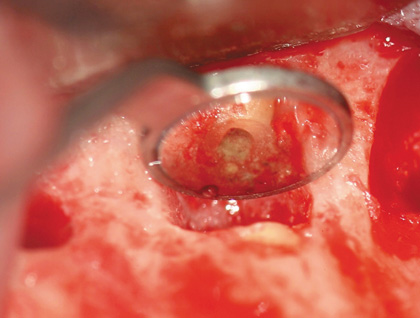
Рис. 10 Ретроградное пломбирование зуба 12 MTI-H
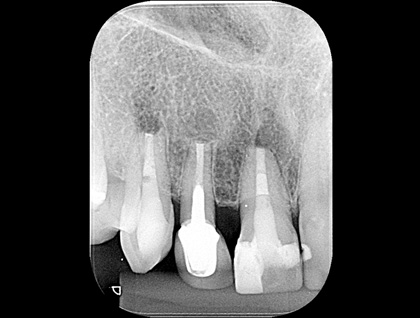
Рис. 11 Послеоперационная рентгенография
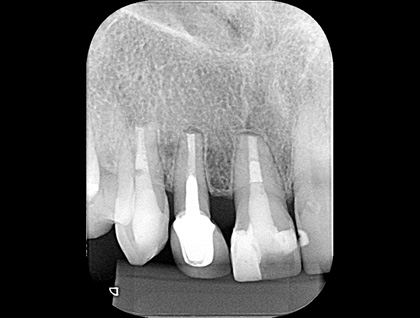
Рис. 12 Контрольная радиография через 5 мес, демонстрирующая переапикальное заживление
Механическое препарирование и биохимическая обработка системы корневых каналов имеет первостепенное значение для успеха эндодонтического лечения. Процедурные ошибки, в том числе смещение апикального отверстия, могут поставить под угрозу позитивный прогноз лечения. Поэтому крайне важно их предотвратить. Рентгенографический и клинический контроль после операции в данном клиническом
случае показали, что микрохирургическая комбинированная методика лечения безопасна, ее результаты предсказуемы.
Координаты для связи с автором:
leandroapp@gmail.com – Леандро А.П. Перейра
1. Al-Sudani D., Al-Shahrani S. A comparison of the canal centering ability of ProFile, K3, and RaCe Nickel Titanium rotary systems. – J. Endod., 2006, v. 32, № 12. – P. 1198–1201.
2. Camara A.C., Aguiar C.M., De Figueiredo J.A. Assessment of the Deviation after Biomechan- ical Preparation of the Coronal, Middle, and Apical Thirds of Root Canals Instrumented with Three HERO
Rotary Systems. – J. Endod., 2007, v. 33, № 12. – P. 1460–1463.
3. Fogarty T.J., Montgomery S. Effect of preflaring on canal transportation: Evaluation of ultrasonic, sonic, and conventional techniques. – Oral Surg. Oral Med. Oral Pathol., 1991, v. 72, № 3. – P. 345–350.
4. Gergi R., Rjeily J.A., Sader J. eta l. Comparison of canal transportation and cen- tering ability of twisted files, Pathfile- ProTaper system, and stainless steel hand K- files by using computed tomography. – J. Endod., 2010, v. 36, № 5. – P. 904–907.
5. Gluskin A.H., Peters C.I., Wong R.D. et al. Retreatment of nonhealing endodontic therapy and management of mishaps .// In: Ingle J.I., Bakland L.K., Baumgartner C. Text book of Endodontics. – USA, Hamilton, Ontario: BC Decker, 2008. – P. 1088–1161.
6. Imura N., Pinheiro E.T., Gomes B.P.F. et al. The outcome of endodontic treatment: a retrospective study of 2000 cases performed by a specialist. – J. Endod., 2007, v. 33, № 11. – P. 1278–1282.
7. Lazarski M., Walker W., Flores C. et al. Epidemiological evaluation of the outcomes of non-surgical root canal treatment in a large cohort of insured dental patients. – J. Endod., 2001, v. 27, № 12. – P. 791–796.
8. Nair P.N., Sjogren U., Krey G. et al. Intraradicular bacteria and fungi in root-filled, asymptomatic human teeth with therapy-resistant periapical lesions: a long-term light and electron microscopic follow-up study. – J. Endod., 1990, v. 16. – P. 580–588.
9. Shuping G., Orstavik D., Sigurdsson A. et al. Reduction of intracanal bacteria using nickel-titanium rotary instrumentation and various medications. – J. Endod., 2000, v. 26. – P. 751–755.
10. Siqueira J., Lima K., Magalhaes F. et al. Mechanical reduction of the bacterial population in the root canal by three instrumentation techniques. – J. Endod., 1999, v. 25. – P. 332–335.
11. Sjogren U., Hagglund B., Sundqvist G. et al. Factors affecting the long-term results of endodontic treatment. – J. Endod., 1990, v. 16. – P. 498–504.
12. Wu M., Fan B., Wesselink P.R. Apical Transportation and Leakage. – J. Endod., 2000, v. 26, № 4. – P. 29–33.
