Journal of Oral Science, 2008. v. 50, № 4, р. 397–402.
Элизабет А. Кулаузиду,
Николаос Экономидес,
Панайотис Белтес
Кафедра терапевтической стоматологии стоматологического факультета Университета Аристотеля в Салониках (Греция)
Джордж Геромихалос,
Константинос Папазисис
Институт рака Theagenion (Салоники, Греция)
Оценка цитотоксичности материалов ProRoot MTA и MTA Angelusinvitro
Резюме
В настоящем исследования проводили сравнительный анализ invitro цитотоксического действия двух доступных на стоматологическом рынке MTA цементов ProRoot MTA и MTA Angelus, модифицированного (для эндодонтического лечения) цинкоксид-эвгенольного цемента SuperEBA, стеклоиономерного цемента светового отверждения Vitrebond на клетки пульпы крысы RPC-C2A и эмбриональные легочные фибробласты человека MRC-5. Клетки культивировали в стандартных условиях, высевали в лунки и подвергали воздействию исследуемыми материалами. Цитотоксическое влияние регистрировали с использованием колориметрической пробы восстановления тетразолиевой соли (XTT метод) через 24 и 72 ч и сравнивали с показателями контрольных групп. В целом степень цитотоксического воздействия в порядке возрастания выглядела следующим образом: ProRoot MTA – MTA Angelus
Введение
Цемент минерал триоксид агрегат (MTA) был предложен для использования в качестве материала для ретроградного пломбирования [2, 35], закрытия латеральных перфораций и перфораций в области фуркации [27], апексификации несформированных верхушек и обтурации системы корневого канала [5, 21]. Применение MTA эффективно также для прямого покрытия пульпы, так как цемент стимулирует образование заместительного дентина, обеспечивая нормальный процесс заживления пульпы [20, 36]. Основа материала – портландцемент, в который для улучшения рентгеноконтрастности добавлен оксид висмута. На стоматологическом рынке представлены MTA цементы двух марок: ProRoot MTA и MTA Angelus, появившийся не так давно. Ряд исследователей описывают биологическое действие ProRoot MTA, но сравнительной оценке биосовместимости ProRoot MTA и MTA Angelus посвящено немного научных статей [1, 29, 33].
При случайном вскрытии полости зуба во время стоматологического лечения возможно защитное покрытие пульпы для сохранения ее жизнеспособности, заживления и восстановления функции. На выбор биологического метода лечения влияет возраст пациента, стадия формирования корня, размер повреждения, микробная обсемененность и т.д.
За последние годы было предложено несколько материалов для защитного покрытия пульпы, такие как цинкоксид-эвгенольный цемент, цементы на основе гидроксида кальция, традиционные стеклоиономерные цементы, а также стеклоиономерные цементы, модифицированные композитной смолой, характеризующиеся улучшенными физико-механическими свойствами [37].
К недавно разработанным материалам для покрытия пульпы зуба можно отнести цементы MTA, стимулирующие репаративные процессы в тканях пульпы и формирование дентинного мостика [3, 26, 36].
Исследования на культурах клеток позволяют расширить знания о возможном токсическом действии материалов и спрогнозировать их влияние на человека. Кроме того, тесты invitro легко выполняются, могут проводиться многократно, требуют меньших материальных затрати могут бытьальтернативой экспериментам invivo. Пробы invitro обычно оценивают соотношение общего количества клеток, контактирующих с исследуемыми материалами, к количеству клеток, создающих устойчивую фракцию, т.е. процент жизнеспособных клеток в конце эксперимента.
Цель исследования
Оценка цитотоксического действия на клетки пульпы крысы и эмбриональные легочные фибробласты человека двух доступных на стоматологическом рынке MTA цементов марок ProRoot MTA и MTA Angelus, модифицированного цинкоксид-эвгенольного цемента SuperEBA, стеклоиономерного цемента светового отверждения Vitrebond с использованием теста на жизнеспособность клеток по активности митохондриальной дегидрогеназы.
Материалы и методы
Клеточные линии и условия культивирования
Фибробласты человека MRC-5, полученные из Банка опухолевых тканей Theagenion (Салоники, Греция) и клетки пульпы крысы RPC-C2A, подаренные профессором кафедры фармакологии стоматологического факультета Токийского медико-стоматологического университета (Япония) С. Касугаи, культивировали в один слой в колбах Т-75 (Costar®Corning®), субкультивировали дважды в неделю при температуре 37˚C в условиях 100%-ной относительной влажности в атмосфере с 5%-ным содержанием СО2. Использовали питательную среду Eagle medium в модификации Dulbecco(DMEM, Gibco, Глазго, Великобритания) с добавлением 10% эмбриональной телячьей сыворотки (FBS, Gibco, Глазго, Великобритания), 100 мг/мл стрептомицина и 100 меж. ед./мл пенициллина.
Сросшиеся клетки в логарифмической фазе роста отделяли путем добавления 2–3 мл 0,05%-ного трипсина (Gibco, 1:250) и 0,02%-ного раствораЭДТА и инкубировались в течение 2–5 мин при температуре 37˚C. Для фотометрической оценки клетки высевали в 12-луночные планшеты Transwell (Costar-Corning, Кембридж) со средней плотностью 30 тыс. клеток на лунку и помещали в инкубатор на 24 ч для достижения экспоненциального роста.
Подготовка исследуемых материалов
Исследовали следующие материалы: белый ProRoot MTA (Dentsply, Йорк, Пенсильвания, США); белый MTA Angelus (Angelus, Лондрина, Бразилия); SuperEBA (Bosworth Co., Skokie, Иллинойс, США); Vitrebond (3M/ESPE, С-Пол, МС, США).
Все материалы готовили согласно инструкциям производителя и вносили на дно погружных лунок 12-луночного планшета Transwell, разграниченных мембранным фильтром с диаметром пор 0,4 мм.После чего погружные лункиподвергали воздействию УФ-облучения (180 Дж/cм2), размещали в лунки с культурами клеток и инкубировали 24 или 72 ч.
Для каждого материала было изготовлено шесть лунок. Контролем служили 12-луночные планшеты с клетками без образцов материалов. По истечении времени экспозиции погружные лунки вынимали и оценивали количество клеток с помощью ХТТ пробы 2,3 бис (2-метокси-4-нитро-5-[(сульфаниламино)карбонил]-2Н-тетразолиум гидроксида).
ХТТ проба
Пробу XTT проводили в соответствии с имеющимися описаниями методики [25, 30]: 500 мл раствора (100:1) XTT (1 мг/мл) (Sigma Chemical Co, С-Луи, МО, США) с 10mMвитамина К3 (MEN) добавляли в лунки, содержащие 2 мл культуральных клеток в питательной среде, планшеты инкубировали 4 ч при температуре 37˚C. Оптическую плотность оценивали в фотометре c титрационным микропланшетомElisa (Anthos 2001) при длине волны 450 нм за вычетом фонового измерения в 620 нм.
Показатель оптической плотности (ОП) рассчитывали как разность между средними значениями спектрального поглощения каждой лунки и регистрационными значениями (оптическая плотность контрольных образцов лунок). Результаты выражали в доле выживаемости, рассчитываемой по формуле: ОПтест/ОПконтроль) х 100%. Среднее значение оптической плотности контрольных лунок, в которые вносили пустые погружные лунки, принимали за 100%.
Для оценки достоверности использовали непараметрические тесты: Крускала–Валлиса и Манна–Уитни с корректировкой Бонферрони (р<0,05).
Результаты и их обсуждение
Каждый эксперимент проводили, по крайней мере, дважды, полученные результаты представлены в таблице 1.
Таблица 1. Показатель цитотоксичности исследуемых материалов на RPC-C2A и MRC-5 клетки при воздействии 24 и 72 ч, выраженный в процентах относительно контрольной группы
| Материал |
Процент жизнеспособных клеток |
|||
|
Время экспозиции, ч |
||||
|
24 |
72 |
24 |
72 |
|
|
RPC—C2A |
MRC-5 |
|||
|
Белый MTA Angelus |
92,49+5,51a* |
88,94+6,81A |
105,39±6,06a |
90,26±3,67A |
|
Белый ProRoot MTA |
91,20±4,62a |
81,84±6,01A |
96,03±4,19a |
92,15±6,74A |
|
Super EBA |
52,37±3,72b |
43,97±3,29B |
63,25±3,98b |
39,00±2,51B |
|
Vitrebond |
15,06±2,88c |
10,43+0,86C |
22,06±5,12c |
19,43±6,29C |
* Указаны средние значения ± СКО. Одинаковые буквы в столбцах обозначают статистически незначимую погрешность (p>0,05).
Фотографии культуральных клеток после экспозиции исследуемых материалов представлены на рисунке 1.



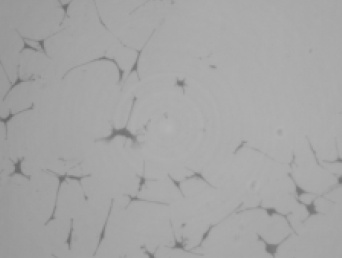
Рис.1 Фотографии культуральных клеток: (a) RPC-C2A при контакте с белым MTA Angelus, (b) RPC-C2A при контакте с белым ProRoot MTA, (c) MRC5 при контакте с SuperEBA, (d) MRC5 при контакте с Vitrebond (увеличение x200)
Расположение материалов в порядке оказываемого цитотоксического действия было следующим: Vitrebond> SuperEBA>ProRoot MTA – MTA Angelus.
ЦементVitrebond показал наивысший показатель цитотоксичности, причем активность митохондриальной дегидрогеназы в клетках RPC-C2A и MRC-5 значительно снижалась через 24 и 72 ч экспозиции. Различия в цитотоксическом действии цементов Vitrebond и SuperEBA были статистически значимы (p<0,05) в обеих линиях культуральных клеток во всех исследуемых периодах.
Сходные результаты получены при нанесении цементов ProRoot MTA и MTA Angelus. В целом оба материала проявили незначительное ингибирующее действие на жизнеспособность клетки. Их влияние было существенно ниже, чем эффект, вызванный контактом с материалами Vitrebond и SuperEBA (р<0,05).
Данные исследования свидетельствуют о биосовместимости цементов MTA Angelus и ProRoot MTA с клетками пульпы крысы и эмбриональными легочными фибробластами человека. Для постановки эксперимента цементы размещали на микропористой мембране в погружных лунках, которые помещали в питательную среду на многолуночковом планшете.Таким образом оценивали влияние образцов на жизнеспособность клеток, исключая физическое взаимодействие между исследуемыми материалами и клетками-мишенями, и сравнивали жизнеспособность клеток в присутствии четырех тестируемых цементов.
RPC-C2A – клональная клеточная линия, созданная из ткани пульпы резца крысы Kasugai и др. [12]. Щелочная фосфатаза клеток RPC-C2A биохимически идентична таковой в клетках пульпы и характеризуется активностью щелочной фосфатазы, являющейся ферментом-маркером для способности к клонированию.Эти клетки обладают высокой пролиферативной активностью и легко культивируютсяв стандартных лабораторных условиях. Данную клеточную линию использовали в нескольких опытах на определение цитотоксичности [14–16]. В настоящем исследовании отобрали также и человеческую клеточную линию MRC-5, чтобы оценить различия в восприимчивости этих двух линий. В действительности оказалось, что клеточная линия RPC-C2A более чувствительны ко всем образцам, чем линия MRC-5, процент жизнеспособных клеток в RPC-C2A повсеместно ниже.
Цементы MTA обеих марок обладают значительно меньшим цитотоксическим действием, чем цементы SuperEBA и Vitrebond. Эти данные подтверждают другие исследования, отмечающие биосовместимость (биоинертность) MTA [11, 16, 17, 23]. Статистически значимых различий между цитотоксичностью MTA Angelus и ProRoot MTA не отмечено. Оба цемента имеют схожий химический состав, хотя ProRoot MTA содержит несколько большую концентрацию оксида висмута [22, 31]. Некоторые авторы оценивали цитотоксическое действие двух MTA цементов и портландцемента на эндотелиальные клетки человека [1]. Никаких статистически значимых различий у всех материалов обнаружено не было, а с увеличением времени экспозиции цитотоксическое действие снижалось. В другом исследовании, в котором воздействию MTA подвергали макрофаги, жизнеспособность наблюдали более чем у 97% клеток во всех опытах как с цементом ProRoot MTA, так и MTA Angelus [29].
Каких-либо данных о цитотоксичности MTA Angelus в пульпе зуба опубликовано не было. Настоящее исследование показало, что MTA Angelus обладает незначительным цитотоксическим воздействием на клетки пульпы (RPC-C2A). Полученные результаты подтверждают биологическую совместимость MTA Angelus и соответствуют данным двух других исследований, посвященных тестированию воздействия этого цемента на эндотелиальные клетки и макрофаги [1, 29].
В настоящем эксперименте исследовали состав белого MTA. Его разработали для клинической практики с целью предотвращения дисколоритов зубов, отмечающихся при применении классического серого MTA. Как белый, так и серый MTA имеют схожее цитотоксическое действие [9] и при покрытии пульпы способствуют ее заживлению и формированию дентинного мостика [19].
Цемент SuperEBA состоит из порошка, содержащего окись цинка (60–75%), кварцевое стекло или оксид алюминия (20–35%), гидрогенизированную смолу (6%) и жидкость, состоящую из 63% этоксибензольной кислоты (EBA) и 37% эвгенола. EBA способствует образованию кристаллической структуры, что повышает прочность материала. Цинкоксид-эвгенольные цементы склонны вызывать воспалительные реакции, главным образом из-за присутствия свободного эвгенола. Результаты ряда исследований свидетельствуют о цитотоксическом влиянии SuperEBA, напрямую связанным с содержанием в его составе эвгенола. Эвгенол широко использовали как антимикробное и противовоспалительное средство. Однако предыдущие исследования in vitro и in vivo продемонстрировали его токсическое действие [4, 6, 8, 13, 10, 18]. Отмечалось, что эвгенол ингибирует миграцию клеток, синтез простагландина, тканевое дыхание и митохондриальную активность [4, 6, 10]. Он также видоизменяет клеточную мембрану [4] и стимулирует нейтрофилы [10, 18].
Vitrebond оказался самым агрессивным среди тестируемых материалов во всех проводимых опытах. Стеклоиономерные цементы, модифицированные композитной смолой, показали повышенную цитотоксичность, что подтверждено результатами нескольких исследований. Некоторые авторы оценивали эффект трех стеклоиономерных цементов, модифицированных композитной смолой, при контакте с культуральными клетками MDPC-23 или подкожном вживлении крысам [32]. Материалы вызвали заметную воспалительную реакцию при прямом контакте с соединительной тканью, а Vitrebond продемонстрировал самое высокое цитотоксическое действие. Добавление выщелачиваемых компонентов смолы, таких как 2-гидроксиэтилметакрилат (HEMA), в композитные смолы, по-видимому, является причиной их цитотоксичности [28]. HEMA – гидрофильньный мономер, легко растворимый в воде. Vitrebond выделяет очень большое количество HEMA после погружения в дистиллированную воду, даже после его фотополимеризации [24]. Он способен подавлять пролиферацию и рост клеток [7], может вызывать их некроз, посредством индукции апоптоза в культивируемых фибробластах [34].
Вывод
В рамках условий данного эксперимента ProRoot MTA и MTA Angelus оказывали сходное положительное воздействие на митохондриальную активность фибробластов. Несмотря на то что результаты исследования in vitro нельзя непосредственно перенести на условия in vivo, оба цемента могут быть рекомендованы для применения в клинической практике.
Авторы выражают благодарность профессору С. Касугаи за предоставленную клеточную линию RPC-C2A.
Список литературы
-
- De Deus G., Ximenes R., Gurgel-Filho E.D. et al. Cytotoxicity of MTA and Portland cement on human ECV 304 endothelial cells. – Int. Endod. J., 2005, v. 38, p. 604–609.
- Economides N., Pantelidou O., Kokkas A. et al. Short-term periradicular tissue response tomineral trioxide aggregate (MTA) as root-end filling material. – Int. Endod. J., 2003, v. 36, p. 44–48.
- Faraco E.V.I. Jr., Holland R. Response of the pulp of dogs to capping with mineral trioxide aggregate or a calcium hydroxide cement. – Dent. Traumatol., 2001, v. 17, p. 163–166.
- Fujisawa S., Kadoma Y., Kodama Y. ‘H and 13C NMR studies of the interaction of eugenol, phenol and triethleneglycol dimethacrylate with phospholipid liposomes as a model system for odontoblast membranes. – J. Dent. Res., 1988, v. 67, p. 1438–1441.
- Gaitonde P., Bishop K. Apexification with mineral trioxide aggregate: an overview of the material and technique. – Eur. J. Prosthodont. Restor. Dent., 2007, v. 15, p. 41–45.
- Gerosa R., Borin M., Menegazzi G., Puttini M. et al. In vitro evaluation of the cytotoxicity of pure eugenol. – J. Endod., 1996, v. 22, p. 532–534.
- Hanks C.T., Strawn S.E., Wataha J.C. et al. Cytotoxic effects of resin components on cultured mammalian fibroblasts. – J. Dent. Res., 1991, v. 70, p. 1450–1455.
- Ho Y.C., Huang F.M., Chang Y.C. Mechanisms of cytotoxicity of eugenol in human osteoblastic cells in vitro. – Int. Endod. J., 2006, v. 39, p. 389–393.
- Holland R., Souza V., Nery M.J. et al. Reaction of rat connective tissue to implanted dentin tubes filled with a white mineral trioxide aggregate. – Braz. Dent. J., 2002, v. 13, p. 23–26.
- Hume W.R. In vitro studies of the local pharmacodynamics, pharmacology and toxicology of eugenol and zinc oxide-eugenol. – Int. Endod. J., 1988, v. 21, p. 130–134.
- Karimjee C.K., Koka S., Rallis D.M. et al. Cellular toxicity of mineral trioxide aggregate mixed with an alternative delivery vehicle. – Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod., 2006, v. 102, p. 115–120.
- Kasugai S., Adachi M., Ogura H. Establishment and characterization of a clonal cell line (RPC-C2A) from dental pulp of the rat incisor. – Arch. Oral Biol., 1988, v. 33, p. 887–891.
- Kasugai S., Hasegawa N., Ogura H. Application of the MTT colorimetric assay to measure cytotoxic effects of phenolic compounds on established rat dental pulp cells. – J. Dent. Res., 1991, v.70, p. 127–130.
- Koulaouzidou E.A., Helvatjoglu-Antoniades M., Palaghias G. et al. Cytotoxicity evaluation of an antibacterial dentin adhesive system on established cell lines. – J. Biomed. Mater. Res. B Appl. Biomater., 2008, v. 84, p. 271–276.
- Koulaouzidou E.A., Papazisis K.T., Beltes P. et al. Cytotoxicity of three resin-based root canal sealers: an in vitro evaluation. – Endod. Dent. Traumatol., 1998, v. 14, p. 182–185.
- Koulaouzidou E.A., Papazisis K.T., Economides N.A. et al. Antiproliferative effect of mineral trioxide aggregate, zinc oxide-eugenol cement, and glass-ionomer cement against three fibroblastic cell lines. – J. Endod., 2005, v. 31, p. 44–46.
- Lin C.P., Chen Y.J., Lee Y.L. et al. Effects pf root-end filling materials and eugenol on mitochondrial dehydrogenase activity and cytotoxicity to human periodontal ligament fibroblasts. – J. Biomed. Mater. Res. B Appl. Biomater., 2004, v. 71, p. 429–440.
- McDonald J.W., Heffner J.E. Eugenol causes oxidant-mediated edema in isolated perfused rabbit lungs. – Am. Rev. Respir. Dis., 1991, v. 143, p. 803–809.
- Menezes R., Bramante C.M., Letra A. et al. Histologic evaluation of pulpotomies in dog using two types of mineral trioxide aggregate and regular and white Portland cements as wound dressings. – Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod., 2004, v. 98, p. 376–379.
- Min K.S., Park H.J., Lee S.K. et al. Effect of mineral trioxide aggregate on dentin bridge formation and expression of dentin sialoprotein and heme oxygenase-1 in human dental pulp. – J. Endod., 2008, v. 34, p. 666–670.
- O’ Sullivan S.M., Hartwell G.R. Obturation of a retained primary mandibular second molar using mineral trioxide aggregate: a case report. – J. Endod., 2001, v. 27, p. 703–705.
- Oliveira M.G., Xavier C.B., Demarco F.F. et al. Comparative chemical study of MTA and Portland cements. – Braz. Dent. J., 2007, v. 18, p. 3–7.
- Osorio R.M., Hefti A., Vertucci F.J. et al. Cytotoxicity of endodontic materials. – J. Endod., 1998, v. 24, p. 91–96.
- Palmer G., Anstice H.M., Pearson G.J. The effect of curing regime on the release of hydroxyetyl methacrylate (HEMA) from resin-modified glass-ionomer cements. – J. Dent., 1999, v. 27, p. 303–311.
- Paull K.D., Shoemaker R.H., Boyd M.R. et al. The synthesis of XTT: anew tetrazolium reagent that is bioreducible to a water-soluble formazan. – J. Heterocycl. Chem., 1988, v. 25, p. 911–914.
- Pitt Ford T.R., Torabinejad M., Abedi H.R. et al. Using mineral trioxide aggregate as a pulp-capping material. – J. Am. Dent. Assoc., 1996, v. 127, p. 1491–1494.
- Pitt Ford T.R., Torabinejad M., McKendry D.J. et al. Use of mineral trioxide aggregate for repair of furcal perforations. – Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod., 1995, v. 79, p. 756–763.
- Ratanasathien S., Wataha J.C., Hanks C.T. et al. Cytotoxic interactive effects of dentin bonding components on mouse fibroblasts. – J. Dent. Res., 1995, v. 74, p. 1602–1606.
- Rezende T.M.B., Vargas D.L., Cardoso F.P. et al. Effect of mineral trioxide aggregate on cytokine production by peritoneal macrophages. – Int. Endod. J., 2005, v. 38, p. 896–903.
- Scudiero D.A,. Shoemaker R.H., Paull K.D. et al. Evaluation of a soluble tetrazolium/formazan assay for cell growth and drug sensitivity in culture using human and other tumor cell lines. – Cancer Res., 1988, v. 48, p. 4827–4833.
- Song J.S., Mante F.K., Romanow W.J. et al. Chemical analysis of powder and set forms of Portland cement, gray ProRoot MTA, white ProRoot MTA, and gray MTA-Angelus. – Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod., 2006, v. 102, p. 809–815.
- Souza P.P.C., Aranha A.M.F., Hebling J. et al. In vitro cytotoxicity and biocompatibility of contemporary resin-modified glass ionomer cements. – Dent. Mater., 2006, v. 22, p. 838–844.
- Souza N.J.A., Justo G.Z., Oliveira C.R et al. Cytotoxicity of materials used in perforation repair tested using the V79 fibroblast cell line and granulocyte-macrophage progenitor cells. – Int. Endod. J., 2006, v. 39, p. 40–47.
- Spagnuolo G., Mauro C., Leonardi A. et al. NF-kappaB protection against apoptosis induced by HEMA. – J. Dent. Res., 2004, v. 83, p. 837–842.
- Torabinejad M., Pitt Ford T.R., McKennedy D.J. et al. Histologic assessment of mineral trioxide aggregate as a root-end filling in monkeys. – J. Endod., 1997, v. 23, p. 225–228.
- Tziafas D., Pantelidou O., Alvanou A. et al. The dentinogenic effect of mineral trioxide aggregate (MTA) in short-term capping experiments. – Int. Endod. J., 2002, v. 35, p. 245–254.
- Van Noort R. Introduction to dental materials. – London: Mosby Elsevier, 2007, p. 127–143.
